
Para comenzar la clase de hoy nuestro profesor nos ha puesto un vídeo llamado Pipas. En él aparecen dos chicas jóvenes hablando. Una de ellas le cuenta a la otra que piensa que su novio le es infiel con una chica llamada Pilar porque el día anterior le dijo - Te quiero Pi-.
Dice que como excusa a su equivocación le a dicho que Pi es un número con decimales infinitos y por eso a ella la quiere infinito, pero no se lo cree. Lo más gracioso del vídeo es que la misma chica lleva una sudadera con el símbolo griego de la letra Pi y piensa que es una letra china.
Este corto nos invita a hacer una reflexión sobre la importancia de la educación, por lo menos general, e invita a motivarse y crecer mentalmente.
Hoy vamos a terminar el tema porque el próximo día 30 tenemos el examen así que el maestro se ha centrado en explicarnos las clasificación de la materia.
Los átomos que forman la materia están situados en el espacio de una manera que permite
explicar las características de los diferentes
estados de agregación.
- Gases: en ellos los átomos se encuentran dispersos y entre ellos existe el vacío. Están en continuo movimiento y ejercen una fuerza sobre las paredes del recipiente que los contiene. Al comprimirlo el vació que existe entre sus átomos se va haciendo más pequeño y de este modo conseguimos que el gas pase a ser líquido.
- Líquidos: El líquido es la materia que ocupa menos volumen. Entre sus átomos posee unos pequeños que permite que este tipo de materia fluya.
- Solido: Es la materia con mayor compresión, sus átomos están mucho mas juntos, prácticamente sin huecos existentes entre ellos lo cual les hace tener siempre un volumen fijo.
Clasificación de la materia en función de si esta formada por uno o varios átomos o si son puros o mezclas
- Mezclas
Son sustancia que pueden separarse con métodos sencillos en otro tipo de sustancias más pequeñas. Las propiedades de las mezclas
pueden variar. En una mezcla podemos encontrar una combinación de dos o más sustancias.Tipos de mezclas:
- Mezclas homogéneas: son aquellas mezclas donde no podemos diferenciar
los componentes de la forma. Algunos ejemplos son cualquier tipo de disolución como : agua y alcohol; agua y sal; o agua y azúcar.
-Mezclas
heterogéneas: son aquellas en las que se pueden distinguir los componentes que la forman. Algunos ejemplos son: agua y
aceite o el granito.
- Sustancia pura
Son aquellas sustancias que no se puede separar mediante métodos sencillos. Siempre tiene las mismas
propiedades y podemos averiguar su densidad, su punto de fusión y su temperatura de ebullición. Las propiedades de una sustancia pura son
invariables. Tipos:
- Sustancias puras
simples: son cada uno de los 118 elementos químicos que conocemos en la actualidad que forman la Tabla periódica. Ejemplos: H, O, He, Al, Fe.

- Sustancias puras
compuestas: compuestos o moléculas que se pueden
formar con la combinación de los elementos químicos de la Tabla periódica. Algunos ejemplos son : Co2 CH4 H2O NH3.
Actividad: ¿Cómo separarías una mezcla formada por agua, arena, sal y limaduras de hierro?
Primero utilizaríamos un imán para atraer todas las limaduras de hierro de la mezcla, en segundo lugar colaríamos la arena mediante un filtro. Y para finalizar tenemos dos opciones: hervimos el agua dando lugar a restos de sal muy finos o dejamos que el agua se evapore a su tiempo dando como resultado sal en cristales cuadrados.
Métodos de
separación sencillos separación de mezclas
- - Filtración: Se utiliza un filtro de papel para hacer pasar un líquido y de este modo las sustancias solidas queden retenidos en él.
- - Imantación: Mediante un imán atraemos las partículas de los metales en las mezclas.
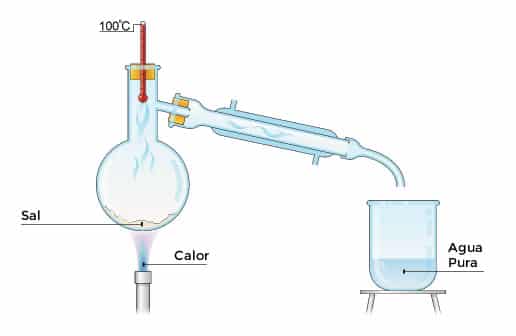 - - Destilación: Método que nos sirve para separar una mezcla de dos líquidos. Lo que se pretende es hervir en un recipiente la mezcla, la sustancia que tenga el punto de ebullición menor pasará a estado gaseoso. Estos vapores llegan a un tubo interior, que se encuentra dentro de otro tubo refrigerante, convirtiendo estos gases de nuevo en líquido y permitiéndonos recogerlo ya separado en
otro recipiente.
- - Destilación: Método que nos sirve para separar una mezcla de dos líquidos. Lo que se pretende es hervir en un recipiente la mezcla, la sustancia que tenga el punto de ebullición menor pasará a estado gaseoso. Estos vapores llegan a un tubo interior, que se encuentra dentro de otro tubo refrigerante, convirtiendo estos gases de nuevo en líquido y permitiéndonos recogerlo ya separado en
otro recipiente.
- - Evaporación: Mediante este método se hierve el líquido pasando a ser vapor y permitiéndonos quedarnos con el sólido. La variación lenta de este método se denomina: cristalización.
 - - Cromatografía: (separación de sustancias como tinta de un rotulador). Introducimos en un recipiente disolvente y una tira de papel de filtro, en ella ponemos una mancha del rotulador sin tocar el disolvente. Poco a poco el disolvente irá subiendo por capilaridad (huecos que se generan en la superficie) y arrastrara las
moléculas hacia arriba.
- - Cromatografía: (separación de sustancias como tinta de un rotulador). Introducimos en un recipiente disolvente y una tira de papel de filtro, en ella ponemos una mancha del rotulador sin tocar el disolvente. Poco a poco el disolvente irá subiendo por capilaridad (huecos que se generan en la superficie) y arrastrara las
moléculas hacia arriba.
- Electrosis: Separación de una sustancia pura compuesta mediante una reacción química.
Actividad: ¿ Cómo sabemos que vaso contiene: agua, agua y aceite, agua y alcohol, agua y alcohol etílico y agua y aceite?
En primer lugar distinguiremos el vaso del agua con aceite solo son verlo ya que las sustancias se mantienen separadas al mezclarse.
Para saber que recipiente contiene cada mezcla pondremos a hervir los recipientes para descubrir el punto de ebullición.
El primero que deberá hervir será el del agua y el alcohol, puesto que el alcohol hierve a 68 grados y por ultimo sabremos cual es el del agua cuando la sustancia hierva al llegar a los 100 grados.
Actividad: ¿Cómo puede explicarse la existencia de un centenar
de sustancias simples y millones de compuestos?
Por la combinación de las 118 sustancias simples que conocemos, de dos en dos o
de tres en tres.
No hay comentarios:
Publicar un comentario